课程内容
第三单元《物质构成的奥秘》课题2 原子的结构(3)
原子有多小
原子的实际质量
一个碳原子的质量:1.993×10-26kg
一个氧原子的质量:2.657×10-26kg
不同原子的质量各不相同,可以用现代科学仪器精确地测量出来。如:
一个氢原子的质量是:1.67×10-27kg,
一个氧原子的质量是:2.657×10-26kg,
一个铁原子的质量是:9.288×10-26kg。
这样小的数字,书写、记忆和使用起来都很不方便,就像用吨做单位来表示一粒稻谷或小麦的质量一样,能不能用一种好写、好记、好用的方法来表示原子的质量呢?
相对原子质量
原子的质量非常小,使用起来很繁琐,不方便,一般不采用。为方便使用确定了原子的相对质量——相对原子质量(Ar)
一、定义
定义:国际上一致同意以一种碳原子质量的1/12作为标准,其他原子的质量跟它比值,就是这种原子的相对原子质量。
碳-12:是含有6个质子和6个中子的碳原子。
二、公式
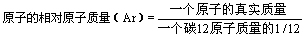
练习:已知1个碳原子的质量是1.993×10-26Kg,一个氧原子的质量是2.657×10-26Kg,求氧原子的相对原子质量?
三、原子质量和相对原子质量的关系
(1)相对原子质量不等于原子的实际质量
(是个比值,相对值) (绝对值)
(2)原子实际质量越大,它的相对原子质量越大
(3)相对原子质量的单位是:“1”
(4)原子实际质量的单位是:千克
相对原子质量与质子数和中子数的关系
相对原子质量=质子数+中子数
质子数
中子数
相对原子质量近似值
氢
1
0
1
碳
6
6
12
氧
8
8
16
钠
11
12
23
铁
26
30
56
原子中各粒子的质量:
推导 原子的质量≈质子质量+中子质量
粒子种类
质量(千克)
相对质量
质子
1.6726×10-27
1
中子
1.6749×10-27
1
电子
质子质量的1/1836
可忽略
相对原子质量
≈质子相对总质量+中子的相对总质量
≈质子数×1+中子数×1
≈质子数+中子数
填写下列表格:
尝试查阅一下如下几种元素的相对原子质量:磷、铝、氮、钠、硫、镁、氯。看谁查得又快又准!
核电荷数
质子数
中子数
电子数
相对原子质量
氢
1
0
1
氦
2
2
氮
7
14
氧
8
16
硫
16
32
铁
26
30
磷——31 铝——27
氮——14 钠——23
硫——32 镁——24
氯——35.5
已知氧原子的质量为aKg,硫原子的质量为bKg,碳12原子的质量为mKg。问:氧原子和硫原子的质量比为a/b;相对原子质量比为a/b。
小结:两种原子的实际质量之比等于他们的相对原子质量之比
练习题
一个铁原子的质量是9.288×10-26kg。请计算出氢原子的质量?(已知氢原子和铁原子的相对原子质量分别是1和56)
课堂小结
相对原子质量
1、引入的原因
2、定义
3、
4、与原子质量的区别
5、相对原子质量=质子数+中子数
我能行
1、据报道,上海某医院正研究用放射碘治疗肿瘤,这种碘原子的核电荷数为53,相对原子质量是125,下列关于这种原子的说法错误的是( )
A、质子数53 B、核外电子数是53
C、中子数53 D、质子数与中子数之和是125
2、贫铀弹的主要成分是低放射性的铀,铀原子的相对原子质量是238,核电荷数为92,中子数应为( )
A、146 B、92 C、136 D、238
3、一个碳原子的质量是1.993×10-26千克,碳的相对原子质量为( )
A、12克 B、14 C、12 D、16
4、镁的相对原子量是24的意义是( )
A、一个镁原子质量是24g
B、一个镁原子质量是一个碳原子质量的24倍
C、一个镁原子有24个质子
D、一个镁原子质量是一个碳原子质量的1/12的24倍
5、原子中决定相对原子质量大小的主要微粒是( )
A、质子数和电子数 B、质子数和中子数
C、中子数和电子数 D、核电荷数
6、在同一原子里,其数目相同的是( )
A、中子数和质子数 B、电子数和质子数
C、中子数和电子数 D、质子数和原子质量
7、在分子、原子、原子核、质子、中子、电子等粒子中,找出符合下列条件的粒子,填在相应的横线上。
(1)能保持物质化学性质的粒子是_______
(2)化学变化中的最小粒子是_______
(3)带正电荷的粒子是_______
(4)不显电性的粒子是_______
(5)质量最小的粒子是_______
(6)在同一原子中数目相等的粒子是_______
(7)决定原子质量大小的粒子主要是_______
【开动脑筋】
某原子的质子数为26,中子数比质子数多4,则该原子中所含微粒总数为( )
A、26 B、56 C、82 D、86
此内容正在抓紧时间编辑中,请耐心等待
崔老师
女,中教高级职称
优秀教师。多次被评为市教育局“教学标兵”,教学功底扎实,教学经验丰富。
























