2021年人教版化学九年级上册 第五单元 化学方程式(二)
100分
试卷分数
60分
合格分数
90分钟
答题时间
试卷来源:同桌100学习网

 Fe₃O₄的读法错误的是()
Fe₃O₄的读法错误的是() 2CO₂的说法不正确的是 ()
2CO₂的说法不正确的是 ()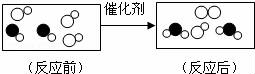
*以下为主观题,系统不自动评分,请答题后自行估分。若没有估分,系统按满分计算。


 Fe₃O₄;(2)2H₂O₂
Fe₃O₄;(2)2H₂O₂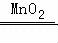 2H₂O+O₂↑;(3)4Al+3O₂
2H₂O+O₂↑;(3)4Al+3O₂ 2Al₂O₃;(4)Zn+2HCl═ZnCl₃+H₃↑;
2Al₂O₃;(4)Zn+2HCl═ZnCl₃+H₃↑; K₂S+3CO₂↑+N₂↑,则S、KNO₃、C完全反应时的质量比为,该配方中C和(填化学式)明显过量。燃放烟花爆竹产生SO₂的反应方程式是。
K₂S+3CO₂↑+N₂↑,则S、KNO₃、C完全反应时的质量比为,该配方中C和(填化学式)明显过量。燃放烟花爆竹产生SO₂的反应方程式是。
 SO₂;(3)2SO₂+O₂
SO₂;(3)2SO₂+O₂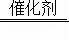 2SO₃;(4)AB;
2SO₃;(4)AB;|
物 质 |
A |
B |
C |
D |
|
反应前质量/g |
4 |
6 |
111 |
4 |
|
反应后质量/g |
待测 |
15 |
0 |
84 |

 _____P₂O₅
_____P₂O₅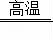 _____Fe+_____CO₂
_____Fe+_____CO₂ _____ KCl+_____O₂↑
_____ KCl+_____O₂↑ _____H₂O+_____CO₂
_____H₂O+_____CO₂


|
加热时间 |
t₁ |
t₂ |
t₃ |
t₄ |
|
剩余固体质量(g) |
4.24 |
4.16 |
4.08 |
4.08 |
