2021年人教版化学九年级下册 第八单元测试卷 (一)
100分
试卷分数
60分
合格分数
90分钟
答题时间
试卷来源:同桌100学习网

|
物质 |
甲 |
乙 |
丙 |
丁 |
|
反应前质量(g) |
4 |
1 |
42 |
10 |
|
反应后质量(g) |
待测 |
20 |
6 |
31 |
*以下为主观题,系统不自动评分,请答题后自行估分。若没有估分,系统按满分计算。

|
金属种类 |
金属质量 |
酸 |
|
铝片 |
1g |
10ml5%稀盐酸 |
|
镁片 |
1g |
10ml5%稀硫酸 |

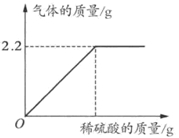

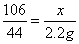
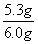 ×100%≈88.3%。
×100%≈88.3%。|
次数 |
加盐酸前 |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
|
加入稀盐酸的质量(g) |
0 |
20 |
20 |
20 |
20 |
20 |
|
锥形瓶内物质的总质量(g) |
11.5 |
31.4 |
m |
71.2 |
91.1 |
111.1 |

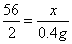 x=11.2g,
x=11.2g,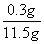 ×100%≈2.6%,2.6%介于2%~4.3%之间,该铁合金属于生铁。
×100%≈2.6%,2.6%介于2%~4.3%之间,该铁合金属于生铁。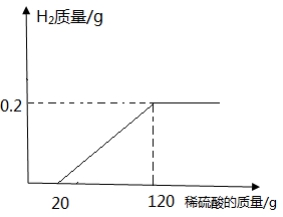

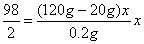 =9.8%
=9.8%


 2Fe+3CO₂
2Fe+3CO₂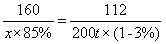


 2Fe+3CO₂
2Fe+3CO₂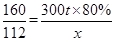 x=168t
x=168t|
|
第一次 |
第二次 |
第三次 |
|
加入稀盐酸的体积(ml) |
15 |
15 |
15 |
|
生成氢气的质量(g) |
0.04 |
m |
0.02 |

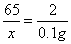
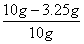 ×100%=67.5% 。
×100%=67.5% 。