2021年人教版化学九年级下册 第九单元测试卷 (一)
100分
试卷分数
60分
合格分数
90分钟
答题时间
试卷来源:同桌100学习网

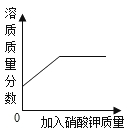
*以下为主观题,系统不自动评分,请答题后自行估分。若没有估分,系统按满分计算。

|
序号 |
温度 |
水的质量 |
所加物质质量 |
溶液质量 |
|
① |
20 |
10 |
2 |
12 |
|
② |
20 |
15 |
2.5 |
a |
|
③ |
20 |
20 |
7 |
26 |
|
④ |
30 |
20 |
7 |
27 |
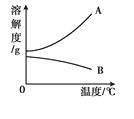

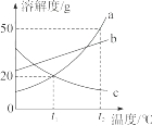

|
实验序号 |
① |
② |
③ |
④ |
|
加入氯化钠的质量/g |
4.5 |
9 |
18 |
20 |
|
溶液质量/g |
54.5 |
59 |
68 |
68 |
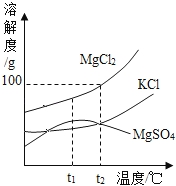


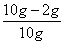 ×100%=80%
×100%=80%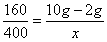 x=20g
x=20g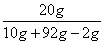 × 100%=20%。
× 100%=20%。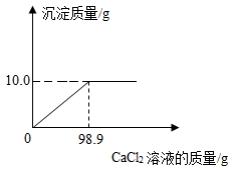

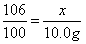 x=10.6g
x=10.6g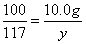 y=11.7g
y=11.7g 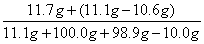 × 100%=6.1%。
× 100%=6.1%。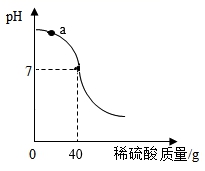

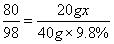

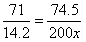 x=7.45%
x=7.45%

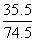





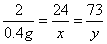
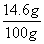 ×100%=14.6%。
×100%=14.6%。|
温度(℃) |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
|
溶解度(g) |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
