2021年人教版化学九年级下册 第九单元测试卷 (二)
100分
试卷分数
60分
合格分数
90分钟
答题时间
试卷来源:同桌100学习网

*以下为主观题,系统不自动评分,请答题后自行估分。若没有估分,系统按满分计算。



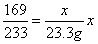 =16.9g,
=16.9g, 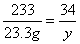 =3.4g
=3.4g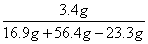 ×100% = 6.8%
×100% = 6.8%
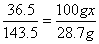 x=7.3%;
x=7.3%;
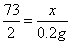 ,
,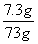 ×100%=10%
×100%=10%|
|
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
|
滴入稀硫酸的质量/g |
25 |
25 |
25 |
25 |
25 |
|
生成气体的总质量/g |
0.05 |
m |
0.15 |
0.20 |
0.20 |

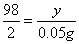
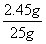 ×100%=9.8%。
×100%=9.8%。 

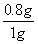 ×100%=80%,
×100%=80%,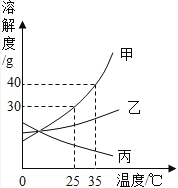


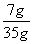 ×100%=20%
×100%=20% |
|
配制方案(只要说明配制时所需的各种药品用量) |
|
方案一 |
|
|
方案二 |
|
|
方案三 |
|

|
|
配制方案(只要说明配制时所需的各种药品用量) |
|
方案一 |
10g食盐溶液,40mL水 |
|
方案二 |
25g40%NaCl溶液,25mL水 |
|
方案三 |
20g15%NaCl溶液,7gNaCl,23mL水 |