2021年人教版化学九年级下册 第十单元测试卷 (一)
100分
试卷分数
60分
合格分数
90分钟
答题时间
试卷来源:同桌100学习网

|
选 项 |
实验目的 |
实验方法 |
|
A |
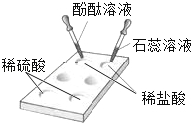
检验一瓶气体是否为氧气 |
将带火星的木条伸入瓶 中 |
|
B |
鉴别 NaOH溶液和稀 H₂SO₄ |
分别滴加紫色石蕊溶液 |
|
C |
除去 CO中混有的 CO₂ |
将混合气体通过灼热的氧化铜粉末 |
|
D |
比较 Fc、 Cu和 Ag的 金属活动性 |
将 Fe和 Ag分别加入CuSO₄溶 液中 |
*以下为主观题,系统不自动评分,请答题后自行估分。若没有估分,系统按满分计算。
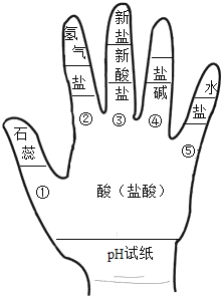


|
实验步骤 |
现象 |
结论 |
|
取上层清液,
|
|
a结论正确 |


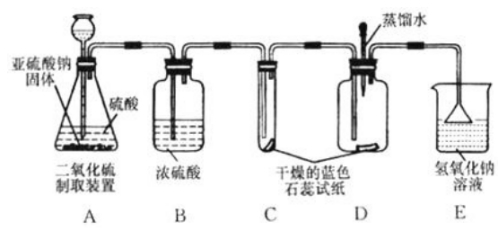

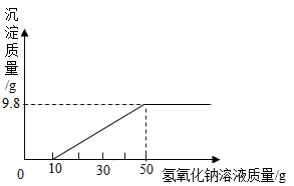

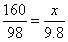
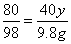

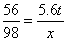 x=9.8t
x=9.8t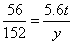 y=15.2t
y=15.2t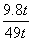 ×100%=20%
×100%=20%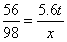 x=9.8t
x=9.8t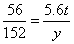 y=15.2t
y=15.2t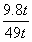 ×100%=20%
×100%=20% 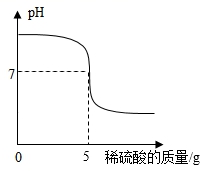

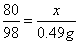 x=0.4g
x=0.4g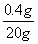 ×100%=2%, 2%>0.001%,所以不能直接排放。
×100%=2%, 2%>0.001%,所以不能直接排放。
|
实验次数 |
1 |
2 |
3 |
4 |
|
加入氯化钡溶液的质量/g |
10 |
10 |
10 |
10 |
|
烧杯中所得溶液的质量/g |
28.03 |
36.06 |
44.09 |
54.09 |

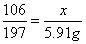 解得:x =3.18g
解得:x =3.18g

|
测定时间 |
5:05 |
5:10 |
5:15 |
5:20 |
5:25 |
5:30 |
5:35 |
|
pH |
4.95 |
4.94 |
4.88 |
4.86 |
4.85 |
4.84 |
4.82 |




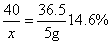
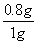 ×100%=80%,
×100%=80%,