2021年人教版化学九年级下册 第十单元测试卷 (二)
100分
试卷分数
60分
合格分数
90分钟
答题时间
试卷来源:同桌100学习网

|
|
性质 |
用途 |
|
A |
氯化钠易溶于水,水溶液有咸味 |
作调味品 |
|
B |
稀盐酸能与某些金属氧化物反应 |
除铁锈 |
|
C |
浓硫酸具有脱水性 |
干燥氧气 |
|
D |
氢氧化钠能与某些非金属氧化物反应 |
吸收二氧化硫 |
*以下为主观题,系统不自动评分,请答题后自行估分。若没有估分,系统按满分计算。




|
实验操作 |
实验现象 |
|
|
|

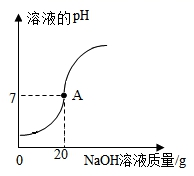

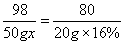 x=7.84%
x=7.84%|
|
第一次 |
第二次 |
第三次 |
第四次 |
第五次 |
|
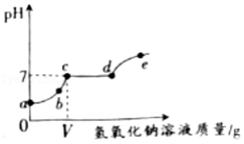
氢氧化钠溶液的质量/g |
20 |
20 |
20 |
20 |
20 |
|
沉淀质量/g |
4.9 |
9.8 |
m |
19.6 |
19.6 |

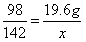 x=28.4g
x=28.4g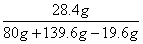 ×100%=14.2%
×100%=14.2%

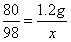 x=1.47g;
x=1.47g;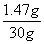 ×100%=4.9%;
×100%=4.9%;|
实验组别 |
一 |
二 |
三 |
四 |
五 |
|
混合溶液质量/g |
100 |
100 |
100 |
100 |
50 |
|
NaOH溶液质量/g |
100 |
150 |
200 |
250 |
100 |
|
沉淀质量/g |
2.9 |
m |
5.8 |
5.8 |
n |




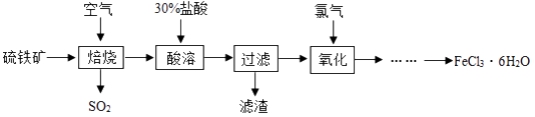

 2Fe₂O₃+8SO₂ 增大反应物接触面积
2Fe₂O₃+8SO₂ 增大反应物接触面积