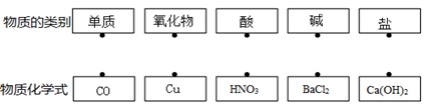
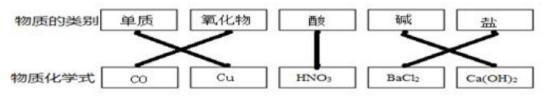
2021年人教版化学九年级下册 第十一单元测试卷 (一)
100分
试卷分数
60分
合格分数
90分钟
答题时间
试卷来源:同桌100学习网

|
序号 |
需区分物质 |
方法一 |
方法二 |
|
A |
浓盐酸和浓硫酸 |
用木条检验 |
闻气味 |
|
B |
氢氧化钠固体和食盐 |
加水 |
加盐酸 |
|
C |
铁粉和炭粉 |
用水搅拌 |
加稀硫酸 |
|
D |
氢氧化钠溶液和氢氧化钙溶液 |
用无色酚酞溶液试液 |
通入CO₂ |
|
|
a |
b |
c |
d |
|
A |
Ba(NO₃)₂ |
HNO₃ |
Ca(NO₃)₂ |
Mg(NO₃)₂ |
|
B |
Ca(NO₃)₂ |
HNO₃ |
M(NO₃)₂ |
Ba(NO₃)₂ |
|
C |
HNO₃ |
Ba(NO₃)₂ |
Ca(NO₃)₂ |
Mg(NO₃)₂ |
|
D |
Mg(NO₃)₂ |
HNO₃ |
Ba(NO₃)₂ |
Ca(NO₃)₂ |
*以下为主观题,系统不自动评分,请答题后自行估分。若没有估分,系统按满分计算。

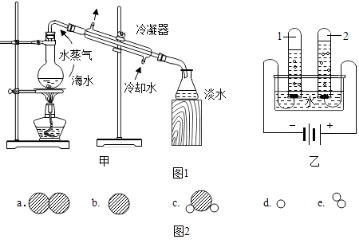
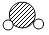 可表示一个水分子)用硬水洗衣服既浪费肥皂也洗不净
可表示一个水分子)用硬水洗衣服既浪费肥皂也洗不净

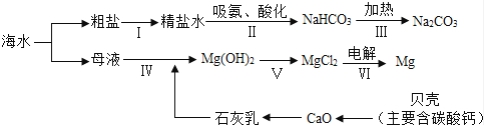

 Na₂CO₃+CO₂↑+H₂O;(6)减少贝壳污染(或提高经济效益、减少资源浪费等其他合理答案也可);
Na₂CO₃+CO₂↑+H₂O;(6)减少贝壳污染(或提高经济效益、减少资源浪费等其他合理答案也可);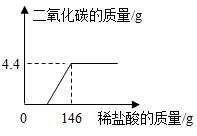

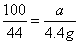 a=10g
a=10g 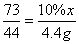 x=73g
x=73g 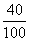 ×100%=4g;
×100%=4g;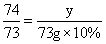 y=7.4g
y=7.4g 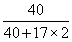 ×100%=4g
×100%=4g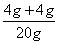 ×100%=40g
×100%=40g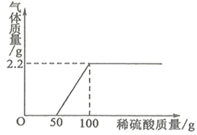

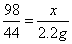 x=4.9g
x=4.9g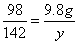

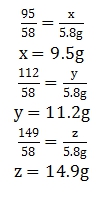
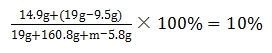
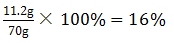 。
。
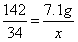 x=1.7g
x=1.7g
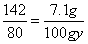 y=4%
y=4%