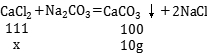2021年人教版化学九年级下册 第十一单元测试卷 (二)
100分
试卷分数
60分
合格分数
90分钟
答题时间
试卷来源:同桌100学习网

|
|
X |
Y |
Z |
Q |
|
反应前的质量/g |
8 |
10 |
1 |
21 |
|
反应后的质量/g |
0 |
21 |
待测 |
9 |


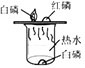
*以下为主观题,系统不自动评分,请答题后自行估分。若没有估分,系统按满分计算。

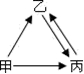

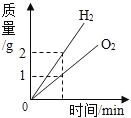
 2H₂↑+O₂↑、两种物质的分子构成不同
2H₂↑+O₂↑、两种物质的分子构成不同|
实验操作 |
预期现象与结论 |
|
步骤1:取少量固体样品于 试管中,加入足量的蒸馏水, 充分振荡。 |
|
|
|
|

 NaCO₃+CO₂↑+H₂O )试计算(写出计算过程);
NaCO₃+CO₂↑+H₂O )试计算(写出计算过程); 
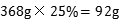 ,根据钠元素在碳酸氢钠中所占质量比,可得碳酸氢钠的质量=
,根据钠元素在碳酸氢钠中所占质量比,可得碳酸氢钠的质量=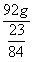 =336g,所以该固体样品中NaHCO₃的质量为336g。
=336g,所以该固体样品中NaHCO₃的质量为336g。 Na₂CO₃+CO₂↑+ H₂O↑
Na₂CO₃+CO₂↑+ H₂O↑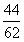 =66g,设该固体样品中NaHCO₃分解了x
=66g,设该固体样品中NaHCO₃分解了x  Na₂CO₃+CO₂↑+ H₂O↑
Na₂CO₃+CO₂↑+ H₂O↑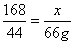 x=252g
x=252g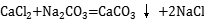
|
次数 |
累计加入氯化钙溶液的质量/g |
烧杯中溶液的总质量/g |
|
一 |
40 |
135 |
|
二 |
80 |
170 |
|
三 |
120 |
205 |
|
四 |
140 |
225 |