2021年人教版化学九年级下册 期中测试卷(一)
100分
试卷分数
60分
合格分数
90分钟
答题时间
试卷来源:同桌100学习网

*以下为主观题,系统不自动评分,请答题后自行估分。若没有估分,系统按满分计算。
 表示钠原子,
表示钠原子, 表示氯原子,
表示氯原子,  表示氧原子)
表示氧原子) 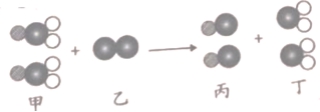

|
实验步骤及操作 |
实验现象 |
|
1.取一支试管,加入约3mL水,再加入1小粒碘充分振荡后静置 |
试管底部有碘固体,液体呈淡黄色 |
|
2.再向上述试管中加入约1mL汽油,充分振荡后静置。 |
试管底部无固体,液体分层,上层呈紫红色,下层接近无色 |


 2CuO
2CuO

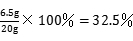
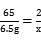

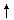
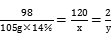
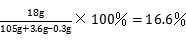
 2Fe+3CO₂。
2Fe+3CO₂。


 ZnSO₄+ H₂↑
ZnSO₄+ H₂↑
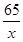 =
=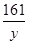 =
= 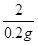
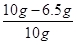 ×100%=35%
×100%=35%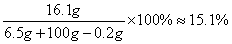





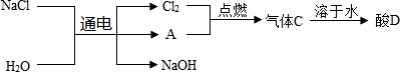
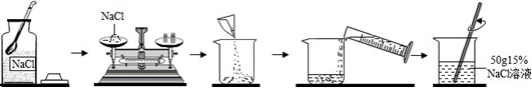

 2NaOH+H₂↑+Cl₂↑ ③HCl
2NaOH+H₂↑+Cl₂↑ ③HCl