2021年人教版化学九年级下册 期中测试卷(二)
100分
试卷分数
60分
合格分数
90分钟
答题时间
试卷来源:同桌100学习网

*以下为主观题,系统不自动评分,请答题后自行估分。若没有估分,系统按满分计算。




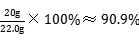 。
。
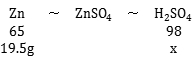
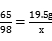 x=29.4g
x=29.4g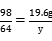 y=12.8g
y=12.8g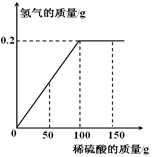

|
|
第一次 |
第二次 |
第三次 |
|
加入稀硫酸的体积(mL) |
15 |
15 |
15 |
|
生成氢气的质量(g) |
m |
0.04 |
0.02 |

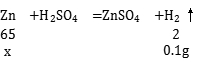
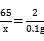 x=3.25g
x=3.25g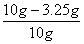 ×100%=67.5%。
×100%=67.5%。




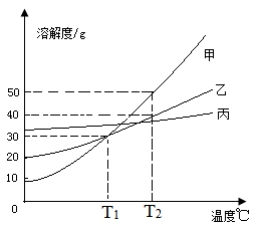
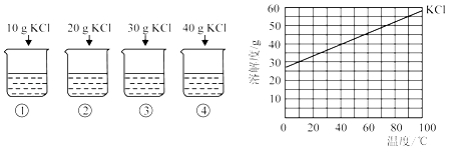
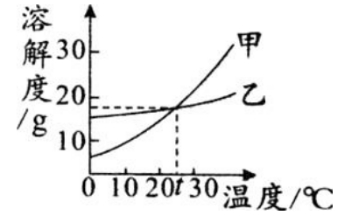
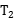 ℃时,向盛有40g甲物质的烧杯中加入50g水,充分溶解后,所得溶液的质量为________g;若将上述溶液降温至
℃时,向盛有40g甲物质的烧杯中加入50g水,充分溶解后,所得溶液的质量为________g;若将上述溶液降温至 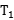 ℃,则此时溶液的溶质质量分数为________(计算结果保留到0.1%)。
℃,则此时溶液的溶质质量分数为________(计算结果保留到0.1%)。 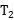 ℃时,甲、乙两种物质的饱和溶液各100g,溶液中所含溶剂的质量甲________乙(填“<”、“>”或“=”)。
℃时,甲、乙两种物质的饱和溶液各100g,溶液中所含溶剂的质量甲________乙(填“<”、“>”或“=”)。
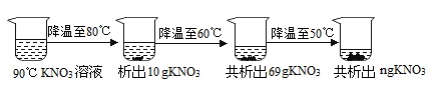
|
温度/℃ |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
|
溶解度/g |
45.8 |
63.9 |
85.5 |
110 |
138 |
169 |
202 |