2021年人教版化学九年级下册 期末测试卷(二)
100分
试卷分数
60分
合格分数
90分钟
答题时间
试卷来源:同桌100学习网

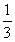 b
b*以下为主观题,系统不自动评分,请答题后自行估分。若没有估分,系统按满分计算。

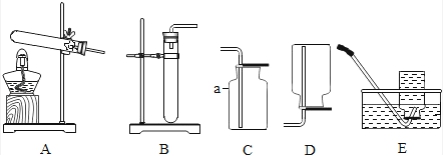
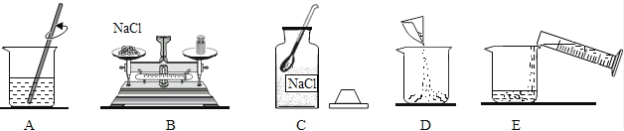

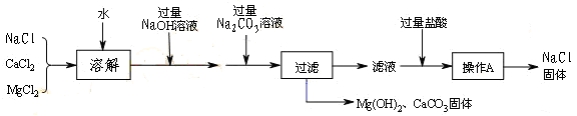
 K₂MnO₄+MnO₂+O₂↑;(3)搅拌加速溶解、CBDEA;
K₂MnO₄+MnO₂+O₂↑;(3)搅拌加速溶解、CBDEA;




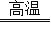 2Fe+3CO₂
2Fe+3CO₂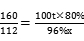 , x≈58t
, x≈58t




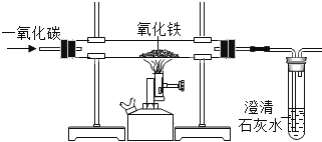

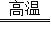 2Fe+3CO₂
2Fe+3CO₂